
Química
AMINAS

Son compuestos orgánicos derivados del amoniaco (NH₃) en el que uno o más átomos de hidrógeno son reemplazados por grupos alquilo o arilo. Se clasifican en tres tipos principales según el número de grupos alquilo unidos al nitrógeno:
Son compuestos orgánicos derivados del amoniaco (NH₃) en el que uno o más átomos de hidrógeno son reemplazados por grupos alquilo o arilo. Se clasifican en tres tipos principales según el número de grupos alquilo unidos al nitrógeno:
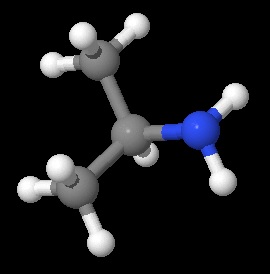
- Aminas primarias (RNH₂): Tienen un solo grupo alquilo. Ejemplo: metilamina (CH₃NH₂).
- Aminas secundarias (R₂NH): Tienen dos grupos alquilo. Ejemplo: dimetilamina ((CH₃)₂NH).
- Aminas terciarias (R₃N): Tienen tres grupos alquilo. Ejemplo: trimetilamina ((CH₃)₃N).
Propiedades
Físicas:
- Solubilidad: Las aminas primarias y secundarias son generalmente solubles en agua, gracias a su capacidad para formar enlaces de hidrógeno. Las aminas terciarias son menos solubles.
- Punto de ebullición: Tienen puntos de ebullición más altos que los hidrocarburos de peso molecular similar debido a la formación de enlaces de hidrógeno entre las moléculas de aminas.
- Olor: Muchas aminas tienen olores fuertes y a menudo desagradables (como el pescado o la orina).
- Estado físico: Las aminas pueden ser gases, líquidos o sólidos, dependiendo de su masa molecular.
Químicas:
- Reacciones de acilo: Reaccionan con cloruros de ácido y anhídridos para formar amidas.
- Reactividad: Pueden reaccionar con ácidos para formar sales de amonio. También participan en reacciones de nucleofilia, atacando compuestos electrofílicos.
- Básicas: Las aminas son bases débiles y pueden aceptar protones (H⁺) debido a la presencia de un par de electrones no compartidos en el nitrógeno.
- Interacciones dipolo-dipolo: Las aminas poseen un momento dipolar debido a la electronegatividad del nitrógeno, lo que influye en su reactividad y propiedades físicas.
- Enlaces de hidrógeno: Las aminas pueden formar enlaces de hidrógeno entre sí y con otras moléculas, lo que afecta sus propiedades de solubilidad y punto de ebullición.

CLASIFICACIÓN
Las aminas se clasifican de acuerdo con el número de átomos de hidrógeno del amoniaco que se sustituyen por grupos orgánicos. Las que tienen un solo grupo se llaman aminas primarias, las que tienen dos se llaman aminas secundarias y las que tienen tres, aminas terciarias.Las aminas sencillas se nombran enumerando los grupos que sustituyen a los átomos de hidrógeno del amoniaco y terminando con amina. Si hay varios grupos o radicales sustituyentes iguales se usan los prefijos di o tri. Cuando se trata de grupos diferentes estos se nombran por orden alfabético (etil antes que metil, o butil antes que propil, prescindiendo del tamaño) y terminando con la terminación amina.
Ejemplos:

Dónde se encuentran
Las aminas como compuestos son muy importantes y reconocidas en industrias como las cosméticas y textiles por el uso o aplicación de la p-Fenilendiamina y algunos derivados se usan en composiciones para teñir el pelo y como antioxidantes para caucho.
- Son parte de los alcaloides que son compuestos complejos que se encuentran en las plantas. Algunos de ellos son la morfina y la nicotina.
- Algunas aminas son biologicamente importantes como la adrenalina y la noradrenalina.
- Las aminas secundarias que se encuentran en las carnes y los pescados o en el humo del tabaco.Estas aminas pueden reaccionar con los nitritos presentes en conservantes empleados en la alimentacion y en plantas, procedentes del uso de fertilizantes, originando N-nitrosoaminas secundarias, que son carcinogenas.
Al degradarse las proteínas se descomponen en distintas aminas, como cadaverina y putrescina entre otras. Las cuales emiten olor desagradable.
- Es por ello que cuando la carne de aves, pescado y res no es preservada mediante refrigeración los microorganismos que se encuentran en ella degradan las proteínas en aminas y se produce un olor desagradable.
